塩化水素ガスを吹き込む実験2015/07/07(火)
少し古い実験書や論文を見ると、「HCl ガスを吹き込む」実験がよく出てきます。こんな反応ですね。
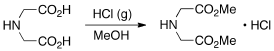
さて、この実験どうやりましょうか。塩化水素ガスをボンベで買ってくる? もちろんそれでもできないことはありませんが、たいてい全量使い切らずにボンベの中に塩化水素ガスが残りますよね。「いつか使うだろうから」とそのボンベをそのまま研究室に放置されると、後々になって処理に難渋することになります(経験あり)。有害ガスを買うんだったら、その実験が終わった時点で、買った人が責任を持って処分してもらわないと困ります。後の世代に託すなんてとんでもない。(と書いたところで思わず「原発ゴミ」のことを思い出しましたが、今日は言いますまい)
ボンベを買わないとすれば、どうすればいいでしょう。よくやるのは、濃硫酸と濃塩酸から HCl ガスを発生させる、という手法です。下のような装置を組み立てます。
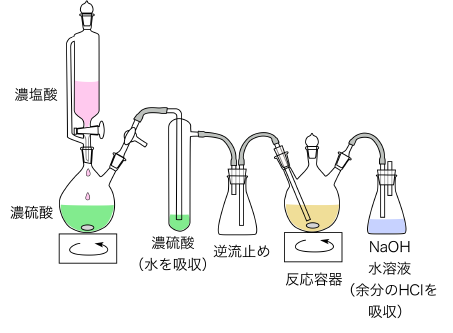
塩酸:硫酸の比率は、モル比で 1:2.8 ぐらいです。実験の時は、もちろん体積に換算して量り取ります。換算した値をここで書くと「モル比を計算しない横着な学生」をアシストすることになるので、やめておきます。
この実験はいくつも注意点があります。初めてやる人は、必ず経験ある指導者に見てもらってください。濃塩酸を滴下すると、激しく発熱して、HCl ガスが盛大に出ます。内圧が急激に上昇しますので、すり合わせの部分は必ずジョイントクリップで止めておきましょう。また、逆流止めや NaOH トラップの「ガラス管の長さ」に注意してください。ガラス管の先がどこにあるかは重要です。逆流止めの入口は、必ず短いガラス管です。NaOH トラップの入口は、長いガラス管で、かつ水面につけないことが大事です。水面につけておくと、反応終了時に HCl の吹き込みをやめた瞬間に、NaOH 溶液が逆流して反応容器に流れ込みます(経験あり)。また、反応容器の吹き込み口が詰まってしまうことがよくあります。この場合、濃塩酸の滴下をやめても発生フラスコの内圧は上がったままになるので、どこかに圧を逃がすコックをつけておく必要があります。
実は、私は最近この実験はほとんどやっていません。上の図も、25年前の実験ノートを引っ張り出して書きました。最近はどうやっているかというと、「HCl を有機溶媒に溶かした溶液」が売られていますので、それを買って使っています。HCl/MeOH, HCl/EtOH, HCl/ジオキサン、HCl/酢酸エチルなどがあります。うちでは国産化学の製品を使うことが多いのですが、他にもあると思います。なんともヘタレな話ですが、上の実験の手間(特に大量に発生する廃酸の処理)を考えると、やむを得ない判断です。化学系の学生だったら一度は「自分で吹き込み」を体験しておいた方がいいような気はするんですけどね。
一つおまけ。この記事を書くために、「塩化水素/エタノール」を検索していたら、ある質問サイトでこんなやりとりを発見。
質問:高校化学の問題です! エタノールに塩化水素を通した時の生成物を答えよ。
答:塩化エチルと水が発生します。
おいおいおいおい。一級アルコールと塩化水素で SN2 かよ。そりゃ無理だろう。長期間放置すれば少しはできるかもしれんけど、実用的な速度では進まないよ。こんな問題を高校化学で出す方も出す方だし、何の迷いもなく答える方も答える方だよ。高校生の皆さん、ネットの質問サイトなんてこのレベルだから、絶対信用しちゃだめだよ。高校化学の先生も、こんな問題を出しているようではダメですよ。しっかりしてくださいね。

